药监局在对无菌类医疗器械生产企业开展GMP现场核查时,厂房的洁净度是其重点检查对象之一。
目前洁净厂房设计主要设计以下法规及标准:- 《医疗器械生产质量管理规范附录无菌医疗器械/植入类医疗器械/体外诊断试剂》;
- 《医疗器械生产质量管理规范无菌医疗器械/植入类医疗器械。体外诊断试剂现场检查指导原则》;
- GB 50073-2001:洁净厂房设计规范;
- GB 50457-2008:医药工业洁净厂房设计规范;
- GB/T 16292-2010:医药工业洁净室(区)悬浮粒子的测试方法;
- GB/T 16294-2010:医药工业洁净室(区)沉降菌的测试方法;
- YY 0033-2000 :无菌医疗器具生产管理规范。
需要对尘埃及微生物含量进行控制的房间(区域)。其建筑结构、装备及其作用均具有减少该房间(区域)内污染源的介入、产生和滞留的功能。
何为洁净度?
洁净环境内单位体积空气内含有大于或等于某一粒径的悬浮粒子的允许统计数。洁净度级别表
| 洁净度级别 | 尘粒最大允许数/立方米 | 微生物最大允许数 | ||
| ≥0.5um | ≥5um | 浮游菌/立方米 | 浮游菌/皿 | |
| 100级 | 3,500 | 0 | 5 | 1 |
| 10,000级 | 350,000 | 2,000 | 100 | 3 |
| 100,000级 | 3,500,000 | 20,000 | 500 | 10 |
| 300,000级 | 10,500,000 | 10,500,000 | - | 15 |
洁净度级别设置原则:
| 产品 | 洁净度级别 |
| 植入和介入到血管的器械:如血管支架 不清洗零部件的加工;末道清洗及组装;处包装及其封口;等 | 不低于10,000级 |
| 植入到人体组织的器械:如起搏器,人工关节 不清洗零部件的加工;末道清洗及组装;初包装及其封口;等 | 不低于100,000级 |
| 与人体损伤表面和粘膜接触的器械:如溃疡敷料等 不清洗零部件的加工;末道清洗及组装;初包装及其封口;等 | 不低于300,000级 |
| 对有要求或无菌操作技术加工的,如血管支架涂药 | 在10,000级下局部100级洁净区内 |
| 注: 如果初包装材料不与器械直接相接触,可以在不低于300,000级下包装。 洁净工作服清洗、干燥和穿洁净工作服室、专用工位器具的末道清洗与消毒的区域的空气洁净度级别可低于生产区一个级别。 | |
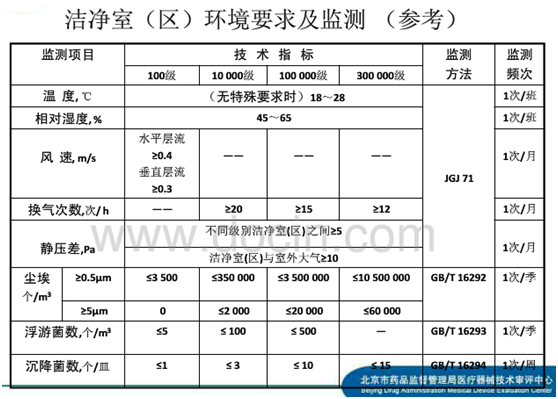
洁净室的控制参数:
- 悬浮颗粒和微生物
- 温度和相对湿度
- 换气次数
- 工作面截面风速
- 压差
- 噪音
- 新风量
- 自净时间