什么是新食品原料(新资源食品)?
新食品原料是指在我国无传统食用习惯的以下物品:
动物、植物和微生物;
从动物、植物和微生物中分离的成分;
原有结构发生改变的食品成分;
其他新研制的食品原料;
同时,新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
新食品原料(新资源食品)注册申报的相关法律法规如下:
新食品原料(新资源食品)注册申报所需的资料:
(一)申请表;
(二)新食品原料研制报告;
(三)安全性评估报告;
(四)生产工艺;
(五)执行的相关标准(包括安全要求、质量规格、检验方法等);
(六)标签及说明书;
(七)国内外研究利用情况和相关安全性评估资料;
(八)申报委托书(委托代理申报时提供);
(九)有助于评审的其他资料。
另附未启封最小包装的样品1件或者原料30克。申请进口新食品原料(新资源食品)的,除了提交上述规定的材料外,还应当提交以下材料:
(一)进口新食品原料出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料;
(二)进口新食品原料生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。
新食品原料(新资源食品)注册申报涉及的测试项目(安全性评估报告)
1.成分分析报告:包括主要成分和可能的有害成分检测结果及检测方法;
2. 卫生学检验报告:3批有代表性样品的污染物和微生物的检测结果及方法;
3. 毒理学评价报告(不同情况下所需提交的毒理学资料不同,请看下表)
4. 微生物耐药性试验报告和产毒能力试验报告(仅适用于微生物类新食品原料);
5. 安全性评估意见:按照危害因子识别、危害特征描述、暴露评估、危险性特征描述的原则和方法进行。
所需 试验 | 国内外均无传统食用习惯的(不包括微生物类) | 仅在国外个别国家或国内局部地区有食用习惯的(不包括微生物类) | 已在多个国家批准广泛使用的(不包括微生物类) | 国内外均无食用习惯的微生物 | 仅在国外个别国家或国内局部地区有食用习惯的微生物类 | 已在多个国家批准食用的微生物类 |
急性经口毒性试验 | 需要提交 | 需要提交 | 需要提交 | - | - | - |
三项遗传毒性试验 | 需要提交 | 需要提交 | 需要提交 | 需要提交 | 需要提交 | - |
90天经口毒性试验 | 需要提交 | 需要提交 | - | 需要提交 | 需要提交 | - |
28天经口毒性试验 | - | - | 需要提交 | - | - | - |
致畸试验和生殖毒性试验 | 需要提交 | 需要提交 | - | 需要提交 | - | - |
慢性毒性和致癌试验 | 需要提交 | - | - | - | - | - |
代谢试验 | 需要提交 | - | - | - | - | - |
急性经口毒性试验 或 致病性试验 | - | - | - | 需要提交 | 需要提交 | 需要提交 |
二项遗传毒性试验 | - | - | - | - | - | 需要提交 |
瑞旭提醒:物质的注册时间与申报材料的准备情况、安全性评估的复杂程度以及审批部门的工作效率等直接相关。一般来说,如果申报材料齐全且符合要求,审批过程可能会相对较快。但如果有需要补充材料或进行进一步测试的情况,注册时间可能会延长。瑞旭建议企业提前制定好所需的材料清单,有序地完成每一项实验。
新食品原料(新资源食品)注册申报流程
瑞旭建议企业在申报新食品原料前,首先应进行可行性评估,确认可行后,方可开展资料编写和试验检测。瑞旭集团对新食品原料的资料准备和行政审批流程做了简单梳理,仅供参考。具体审批流程请于国家卫生健康委员会官方网站查看。
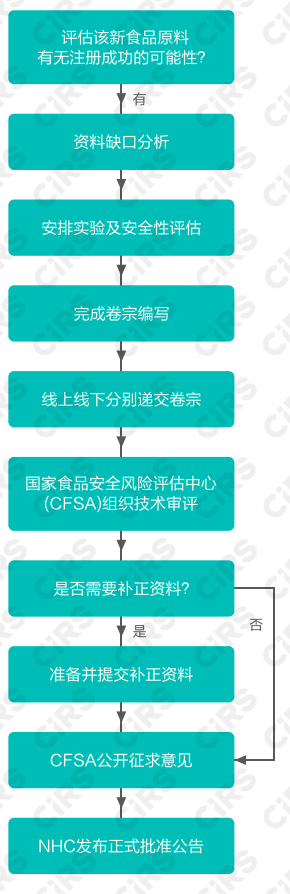
瑞旭提醒:国家鼓励新食品原料的研发与应用,随着新食品原料的申报数量不断增加,国家卫健委的审批速度也在加快。但审评的门槛要要求并未降低,企业在申报的时候应确保资料的完整和科学性,充分节约时间成本,加快审评进度。一般来说,新食品原料申报从受理到正式批准一般需要2~3年的时间。
瑞旭集团新食品原料合规方案
瑞旭集团食品事业部凭借专业技术能力、多方资源和全球网络为客户提供全球新食品申报服务。经验丰富且具有众多成功案例,包括D-阿洛酮糖,3’-SL,富谷胱甘肽酵母、PQQ、梁河滇皂荚等多种新食品原料,项目经验位于行业前列。同时,依托自研平台「食规查」,为企业提供一站式合规管理服务。
我们的服务
- 中国新食品原料注册申报
- 美欧澳等新食品原料申报
- 转基因微生物(遗传修饰微生物)新食品原料申报
为什么选择瑞旭集团
瑞旭集团成立于2007年,集团员工数超450人,总部位于杭州,在美国、英国、爱尔兰、韩国、日本等地拥有11家子公司,可为企业出海提供一站式的全球食品申报注册服务,能高效、稳妥地帮助企业打通市场准入。
瑞旭集团(CIRS Group)凭借着丰富的行业经验、雄厚的技术实力、全球布局以及成功案例等方面的积累,在食品添加剂及“三新食品”申报领域受到广泛关注和企业好评。
- 政府好感度高:瑞旭集团与政府机构保持着长期的良好沟通,能第一时间获取最有价值的国内资源、资讯。
- 拥有丰富的实战经验:瑞旭集团在三新食品申报,特别是在转基因微生物(遗传修饰微生物)和合成生物学产品的申报上,积累了大量成功案例,处于行业前列。
- 高素质的专业技术团队:食品事业部团队中,80%以上的成员拥有食品相关专业硕士及以上学历,团队成员大多拥有10年左右的食品法规服务经验。多人获得中国毒理学会认证毒理学家(DCST)、美国毒理学家(DABT)及欧洲注册毒理学家(ERT)。
- 新原料申报服务能力成功扩展海外:业务范围拓展到欧洲、美国、澳新、日本、韩国、印度、巴西等多国;技术团队具备优秀的英文、日文、韩文等多国语言能力,可提供本地化更精准、优质的服务。
新食品原料(新资源食品)常见问题
问:新食品原料(新资源食品)的审批时间多久?
答:一般来说,新食品原料申报从受理到正式批准一般需要2~3年的时间。
问:若某原料在国外已有获批依据,但生产工艺与国外的不同,申报时毒理学评价试验的选择应该套用无传统食用习惯还是国外个别国家有使用习惯的产品要求?
答:《新食品原料申报与受理规定》中明确规范了物质选择毒理学评价试验的原则,需视物质在国内外的食用情况而定。中国在审批参考国外获批依据时,对物质一致性要求较高(从质量规格、生产工艺多方面进行比较)。若生产工艺与国外产品不同,毒理学等安全性资料需要从严考虑。
问:新食品原料申报对生产工艺是否有限制,获批后使用是否可以更改工艺?
答:新食品原料获批公告中会同步公开生产工艺,可以理解为对生产工艺的限制,不可擅自更改。若企业实际的生产工艺与获批工艺存在出入、或不能符合公告中生产工艺描述,需要重新申报、提交审评。
问:三新食品送检毒理试验的样品与质量规格检测用样品的批次有对应要求吗?
答:申报受理相关法规中均无明确规定。建议毒理学试验所用样品批号为质量规格检测用三批样品之一。
问:获批的新食品原料能否用于特医食品?
不一定。需要根据该原料的批准公告和GB 29922或GB 25596进行综合性判断。
新食品原料的使用需参照批准公告中的使用范围,公告中规定可用于特殊医学用途配方食品时则可作为特医食品原料,公告中未明确说明的,则需要结合特医食品的原料要求具体分析。
问:生产企业在国外的新食品原料可以是国内企业为申请人吗?
答:可以。申请人可以是非生产企业。同时,可以接受申请人与生产企业所在国家不同的情况。例如:申请人为国内企业,而产品由国外工厂生产。申报时,应向审评机构说明两者间的关系。
问:关于实质等同的新原料申报,如果也是需要提供全套的申报材料,那是不是就按照一个全新的原料去申报,这样也不用去跟已经批准的新原料进行比对了,卫健委还会去查那个已经批准的原料信息吗?
答:需要在申报材料中对生产工艺、质量指标、卫生指标等与已经公告内容进行对比。
相关资讯
想了解更多法规相关,请联系我们
联系人:俞经理 13758216434(微信同号)
联系电话:0571-87206538
添加“CIRS食品合规助手”微信,备注企业名称,即可咨询!

