什么是美国GRAS
GRAS是Generally Recognized as Safe(“公认为安全”)的缩写,是美国食品法律中非常重要的一个类别。简单来说,如果一个物质,经过科学培训且具有经验和资质的专家组通过科学程序充分证明其在预期使用条件下是安全的,此物质即为GRAS。
GRAS认证具有较高的国际认可度,是企业为其食品原料或食品添加剂打开国际市场的重要通行证之一。
美国GRAS主要内容
美国GRAS 认证的类型
美国GRAS分为“GRAS自我声明”和“FDA GRAS认证”两类:
① GRAS 自我声明(Self GRAS):
由合格的专家组形成对物质安全性的认可。这类GRAS不向美国FDA提交通报,不经过FDA审核,一般不会对外公开。
② FDA GRAS认证(FDAGRAS Notice):
需要向FDA正式提交,并经过FDA官方审核和批准。若FDA的结论为“没有疑问(FDAhas no questions)”,即可纳入GRAS名单,并且可在FDA官网上查证。经过官方通报,一般来说这类GRAS更具权威性,能得到更广泛的认可。
谁可以申报 GRAS ?
任何个人或机构都可以向FDA提交通报,说明某一物质属于GRAS,从而豁免美国法律要求的上市前审批程序。
关键时间节点:2025年9月4日和2026年1月23日
重要法规更新:
GRAS 认证的一般程序
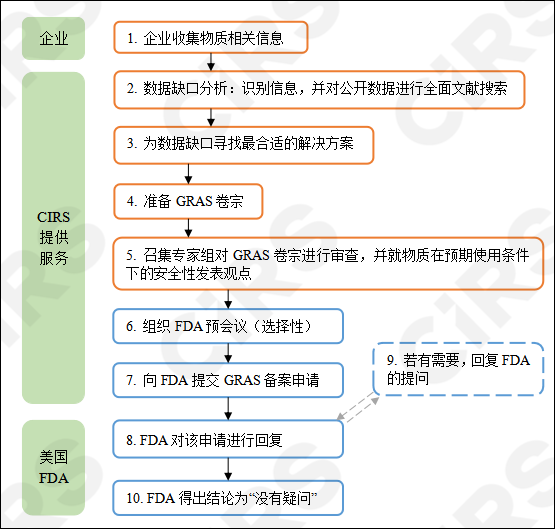
注:前5步为GRAS自我声明的一般程序,后5步在选择向FDA GRAS认证时需进一步开展。
GRAS认证的一般资料
通常情况下,企业需准备以下几方面的资料以供数据分析,同时,瑞旭也会根据物质特性,给每个物质分别准备对应的checklist。
1)物质基础信息:如物质定义,常用名,化学名称或同义词,商品名称,化学结构,相对分子质量等;
2)该物质在食品中的预期用途和使用水平;
3)生产工艺;
4)质量规格及相关分析报告;
5)食品自限性的水平;
6)在食用中使用的历史;
7)安全性阐述。
瑞旭提醒:若食品原料涉及合成生物学技术,也就是通过遗传修饰微生物(转基因微生物)发酵生产的食品原料,需要额外提供基因编辑相关资料,以及生产菌的菌株鉴定、全基因测序及分析等相关资料。
预估周期
主要步骤 | 预估周期 |
数据缺口分析 | 1个月 |
GRAS卷宗准备和提交 | 3-6个月 |
FDA审核 | 6个月(特殊情况下,可延迟至9个月) |
合计 | 10-16个月 |
瑞旭提醒:以上预估周期不包括试验周期。GRAS通常可以引用相同物质的公开数据,包括毒理数据等。若物质比较新,没有公开的毒理数据,则企业需要委托毒理试验,通常周期要增加至少半年。
我们的服务
- 美国GRAS认证咨询及培训
- Self GRAS认证
- FDA GRAS通报
- GRAS资料缺口分析
- 组织FDA官方会议
为什么选择瑞旭?
瑞旭集团成立于2007年,集团员工数超450人,总部位于杭州,在美国、英国、爱尔兰、韩国、日本等地拥有11家子公司,可为企业出海提供一站式的全球新食品原料注册申报服务,能高效、稳妥地帮助企业打通美国食品原料市场准入。
- 美国本地团队:瑞旭美国公司位于弗吉尼亚州,我们拥有全职的美国食品法规专家,提供美国FDA GRAS,NDI,CAP,Animal food GRAS,FDA Animal Food Ingredient Consultation, AAFCO SRIS等合规服务。中美协同,国内项目经理对接 + 美国技术执行,响应快、时差小、沟通顺畅。
- 资深专家阵容:瑞旭集团拥有24位中国毒理学专家(DCST),1位欧洲注册毒理学家(ERT),2位美国毒理学专家(DABT),DABT可作为GRAS专家小组成员,参与会议并签字GRAS卷宗。
- 海量成功案例:瑞旭集团食品事业部有15年以上的食品合规服务经验,拥有众多成功案例,包括母乳低聚糖(2’-FL,LNnt、LNT等)、甜菊糖苷、肌醇、巴西甜蛋白、番茄红素、酶转甜菊糖苷RebM2、NMN、灭活AKK、镰刀菌蛋白、D-阿洛酮糖、氨基葡萄糖盐酸盐、N-乙酰氨基葡萄糖(NAG)、β-胡萝卜素、玉米黄质、虾青素、PQQ等
- 跨领域覆盖:瑞旭集团食品事业部提供全球新食品原料注册申报服务,覆盖20+国家和地区,包括中国、美国、欧洲、澳大利亚、新西兰、加拿大、韩国、日本、巴西、墨西哥、新加坡、马来西亚、泰国、越南、印度尼西亚、台湾地区等。
- 全链条覆盖:从资料梳理、数据 gaps 分析、试验方案设计、专家评审、卷宗编制、到申报递交、后续合规维护全程负责。成熟流程与本地资源,周期更短、费用透明、一次通过率高,减少反复整改成本。
- 长期法规跟踪:持续监控 FDA GRAS 政策变化(如 Self-GRAS 改革趋势),提供长期合规与市场预警。
美国GRAS 认证中企业常见问题:
Q1:Self GRAS和FDA GRAS的区别是什么?
A1:Self GRAS(自我认证GRAS):由企业自行组织专家评审,内部存档,无需向FDA提交。流程简化,节省时间和成本,但不具有FDA的权威背书。FDA GRAS(FDA GRAS Notification):需要向FDA提交材料,经过FDA官方审核。审核通过的物质会在FDA官网公开,更具权威性,适合需要FDA背书的场合。
Q2:一种GRAS物质是否适用于所有用途?
A2:不一定。GRAS认证是基于物质的用途而非物质本身。即使某种物质在某一用途上是GRAS,也不代表它在所有用途上都安全。每种用途都需要经过独立的安全性评估。
Q3:新食品成分能否申报GRAS认证?
A3:可以,但需要根据物质的预期用途和具体成分来判断。例如,如果物质的预期用途是“除了着色以外”的其他用途,且赋予的颜色不明显,则可以进行GRAS认证。如果预期用途包含“着色”,则需要进行着色剂请愿。
Q4:企业是否必须收到FDA的“No questions”答复后才能销售?
A4:不需要。企业可以在不通知FDA的情况下,或者在FDA评估GRAS卷宗的同时,按照其预期用途的条件在美国销售GRAS物质。
Q5:GRAS卷宗如何处理商业秘密问题?
A5:申请FDA GRAS认证意味着申请材料的公开,包括自有实验数据、生产过程参数等可能涉及申请人商业秘密的内容。企业应事先做好预案和权衡,以应对FDA可能的补充材料要求。
Q6:在FDA GRAS通报的过程中会涉及现场核查吗?
A2:不涉及(除非触发特殊安全问题,被FDA关注到)。
Q7:美国FDA对通报GRAS的工厂有什么资质要求吗?
A7:对工厂没有具体的资质要求,但生产上需要符合美国现行GMP的要求。
想了解更多法规相关,请联系我们
联系人:俞经理 13758216434(微信同号)
联系电话:0571-87206538
添加“CIRS食品合规助手”微信,备注企业名称,即可咨询!

