为了指导企业更好地进行保健食品注册和备案工作,保健食品备案管理信息系统和国家市场监督管理总局食品审评中心网站上多次发布保健食品常见问题与解答。瑞旭集团特对这些内容进行汇总和梳理,形成保健食品常见问题与解答系列,供企业查阅。
往期内容回顾:
2、备案稳定性实验如何执行?是否可以委托检测?保健食品常见问题与解答——备案篇(2):理化检验及质量标准
3、进口保健食品备案证明文件怎么出?保健食品常见问题与解答——备案篇(3):进口保健食品备案

本期内容:保健食品常见问题与解答——备案篇(4):其它。
1. 原注册人产品转备案流程(2017-7-4)
答:根据《保健食品备案工作指南(试行)》的要求,原注册人产品转备案的,应向总局保健食品审评中心提出申请。现将原注册人资质确认具体事宜通知如下:
一、申请原注册人资质确认应提交以下资料:
- 变更注册申请表及申请人对申请材料真实性负责的法律责任承诺书 新保健食品注册管理系统上线之前,请在总局保健食品审评中心网站下载专区获取申报模板(点击下载)下载专区/保健食品或(点击下载)/下载专区/保健食品)
- 注册转备案申请书,应由法人代表签字并加盖申请人印章
- 营业执照、统一社会代码/组织代码等申请人主体登记证明文件复印件
- 保健食品注册证书及其附件复印件(未获注册产品免于提供)
二、已获注册的产品转备案申请流程:
已获注册的产品,注册人按变更注册向总局受理部门提出变更申请。
(一) 自本通知发布之日至新保健食品注册管理系统正式上线之前
注册申请人登录保健食品备案管理信息系统(点击注册),点击“获取登录账号”,填写账户信息,并勾选“原注册人”,再填写企业信息及已注册产品信息,将所需资料扫描后上传。已获取登录账号的原注册人,在账户首页点击“注册转备案申请”,填写原注册产品的相关信息,将所需资料扫描后上传。
申请人网上提交后,应同时将盖有公章的一份上述纸质资料原件报送总局行政受理服务部门。
总局审评中心收到纸质资料后进行审核,审核结束后向申请人填写的联系电话发出告知短信,并提示申请人可在备案管理信息系统中查看审核结果。符合原注册人要求的,总局审评中心将原注册产品电子信息转送各省级食品药品监督备案管理部门,各省级局可按规定发放登录账号;已获取登录账号的原注册人可直接在备案管理信息系统中申请产品备案。
(二) 新保健食品注册管理系统正式上线之后
注册人首先在保健食品注册管理系统中按变更注册要求提出“注册转备案”变更申请,在获得国家食品药品监督管理总局确认原注册人资质的《未获批准通知书》后,以原注册人身份向备案管理部门提出备案管理信息系统登录账号申请(已有登录账号的除外)和产品备案申请。
三、《保健食品原料目录》发布之前受理的注册产品申请流程
《保健食品原料目录》(以下简称《原料目录》)发布前受理的新产品注册申请、延续注册申请、变更注册申请、转让技术注册申请,注册申请人可按补充资料要求直接向审评中心提出变更申请,获得原注册人资质确认的可按照第二条相关流程进行产品备案。
四、存在以下情形之一的,不予确认原注册人资质:
(一)不符合《办法》《指南》等对原注册人要求的;
(二)主体证明文件与注册证书相关信息不一致、或未能提供相一致证明材料的;
(三)无特殊原因未在规定时限内提出注册转备案变更申请的;
(四)《原料目录》发布后受理的新产品注册申请,其原料已列入原料目录,且符合备案相关技术要求的;
(五)新产品注册申请已作出不予注册决定的;
(六)因保健功能、安全性和质量可控性等原因已作出不予延续注册决定的;
(七)注册证书存在真实性问题的;
(八)其他不属于注册转备案管理的情形;
本流程自发布之日起施行。
2. 国产保健食品生产企业如何申请备案?(2017-09-28)
答:国产保健食品备案人是生产企业的,可参照下列情况申请登录账号,进行产品备案:
- 备案人未持有符合备案要求的保健食品注册证书的,应直接在备案管理系统中选择备案类型为“国产保健食品”,原注册人选项为“否”。
- 备案人持有符合备案要求的保健食品注册证书的,可以以非原注册人身份申请登录账号后,对新产品进行备案,或对注册转备案产品进行备案;也可以在获得原注册人资质后,以原注册人的身份申请登录账号。
国产保健食品生产企业申请登录账号时,应同时上传生产许可证等主体登记证明文件。
3.同一个产品选用不同的内包装材料时应如何提交备案的相关资料?(2018-03-09)
答:备案人拟选用两种或以上直接接触产品的包装材料时,如果产品新申请备案,除在产品技术要求的“直接接触产品包装材料的种类、名称及标准”中注明不同的包装材料外,还应该对使用不同包装材料生产的产品分别出具相应所有的检验报告。已获得备案凭证的产品拟增加直接接触产品的包装材料时,应该按照备案变更的程序提交相关变更材料。
4. 备案保健食品信息填报流程图(2019-03-26)
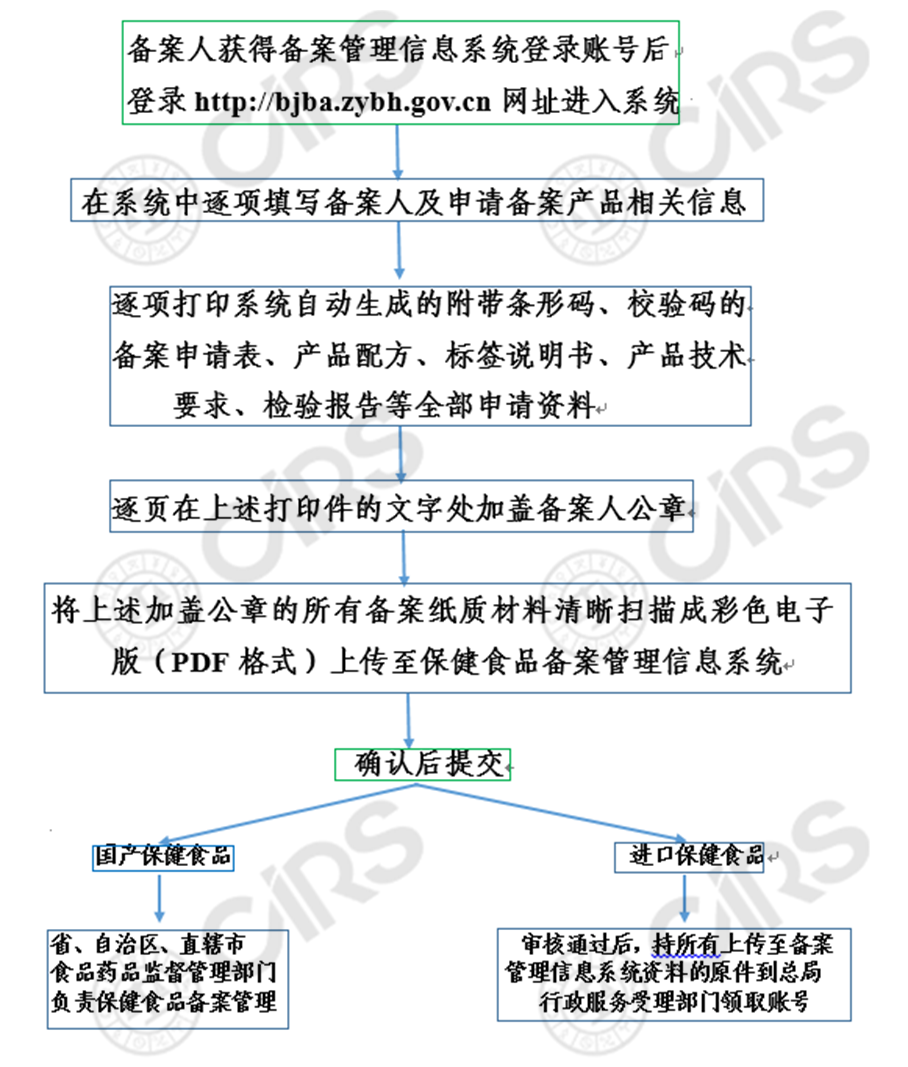
注:
1.问答来源:国家市场监督管理总局保健食品备案管理信息系统;
2.每个问题后括号中备注的日期为国家食品审评中心发布该问答的具体时间,以供参考;
3.“国家食品药品监督管理局”目前已改名为“国家市场监督管理总局”。
相关推荐:
- 保健食品常见问题与解答-备案篇(1):原辅料
- 备案稳定性实验如何执行?是否可以委托检测?保健食品常见问题与解答——备案篇(2):理化检验及质量标准
- 进口保健食品备案证明文件怎么出?保健食品常见问题与解答——备案篇(3):进口保健食品备案
- 定了!境外生产企业注册2个重要节点,2022年1月1日启运,2022年1月1日生产
- 18类外进口食品如何申请境外生产企业注册?
- 2021年上半年保健食品注册类产品批件发布情况分析
- 瑞旭再传捷报!17款进口保健食品备案产品发布,近半数由瑞旭申报成功!
我们的服务:
